.
Ένας τριπλός δεσμός στη χημεία είναι ένας χημικός δεσμός μεταξύ δύο ατόμων που περιλαμβάνει έξι δεσμικά ηλεκτρόνια (bonding electrons) αντί για τα συνηθισμένα δύο σε έναν απλό ομοιοπολικό δεσμό. Ο πιο συνηθισμένος τριπλός δεσμός, που υπάρχει μεταξύ δύο ατόμων άνθρακα, βρίσκεται στα αλκίνια. Άλλες χαρακτηριστικές ομάδες που περιέχουν έναν τριπλό δεσμό είναι τα κυανίδια (νιτρίλια) και τα ισοκυανίδια (ισονιτρίλια). Μερικά διατομικά μόρια, όπως το άζωτο και το μονοξείδιο του άνθρακα έχουν επίσης τριπλούς δεσμούς. Στον σκελετικό τύπο (skeletal formula) ο τριπλός δεσμός σχεδιάζεται με τρεις παράλληλες γραμμές (≡) μεταξύ των δύο συνδεόμενων ατόμων· στην τυπογραφία, αυτό πραγματοποιείται με τον τελεστή ταυτότητας.[1][2][3]
Οι τριπλοί δεσμοί είναι ισχυρότεροι από τους απλούς ή διπλούς δεσμούς και είναι επίσης πιο μικροί. Η τάξη του δεσμού (bond order) είναι τρία.
 |
 |
 |
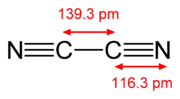
| Αιθίνιο, H−C≡C−H | Δικυάνιο, N≡C−C≡N | Μονοξείδιο του άνθρακα, C≡O |
| Χημικές ενώσεις με τριπλούς δεσμούς | ||
Δεσμοί
Ο τύπος του δεσμού μπορεί να εξηγηθεί με όρους υβριδισμού τροχιακών (orbital hybridization). Στην περίπτωση του αιθινίου κάθε άτομο άνθρακα έχει δύο τροχιακά sp και δύο τροχιακά p. Τα δύο τροχιακά sp είναι γραμμικά με γωνίες 180° και καταλαμβάνουν τον άξονα x στο καρτεσιανό σύστημα συντεταγμένων. Τα τροχιακά p είναι κάθετα στον άξονα y και τον άξονα z. Όταν τα άτομα άνθρακα πλησιάζουν μεταξύ τους τα τροχιακά sp επικαλύπτονται για να σχηματίσουν έναν sp-sp δεσμό σ. Ταυτόχρονα τα τροχιακά pz πλησιάζουν και σχηματίζουν μαζί έναν pz-pz δεσμό π. Παρομοίως, το άλλο ζευγάρι των py-τροχιακών σχηματίζουν έναν py-py δεσμό π. Το αποτέλεσμα είναι ο σχηματισμός ενός σ δεσμού και δύο π δεσμών.
Στον πρότυπο δεσμού κάμψης ο τριπλός δεσμός μπορεί επίσης να σχηματιστεί από την επικάλυψη των τριών sp3 λοβών χωρίς την ανάγκη εφαρμογής ενός π δεσμού.[4]
Παραπομπές
Πρότυπο:JerryMarch
Organic Chemistry 2nd Ed. John McMurry
Pyykkö, Pekka; Riedel, Sebastian; Patzschke, Michael (2005). «Triple-Bond Covalent Radii». Chemistry - A European Journal 11 (12): 3511–20. doi:10.1002/chem.200401299. PMID 15832398.
Advanced Organic Chemistry Carey, Francis A., Sundberg, Richard J. 5th ed. 2007
Μόρια με δακτυλίους έχουν επιπλέον δεσμούς σ, γι' αυτό και προστίθεται ο Nδ. Έτσι, για παράδειγμα το βενζόλιο (C6H6) έχει 12 δεσμούς σ (= 12 άτομα + 1 δακτυλιος - 1) και το μόριο του ανθρακένιου (C14H10) που έχει 3 δακτυλίους, ο κανόνας δίνει σωστά 26 δεσμούς σ (= 24 άτομα + 3 δακτύλιοι - 1). Πιο συγκεκριμένα περιέχει 16 δεσμούς σ C-C και 10 δεσμούς σ C-H.
Hellenica World - Scientific Library
Από τη ελληνική Βικιπαίδεια http://el.wikipedia.org . Όλα τα κείμενα είναι διαθέσιμα υπό την GNU Free Documentation License

